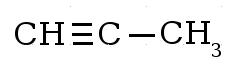COMPOSICIÓN QUÍMICA DE LOS SERES VIVOS I
BIOELEMENTOS
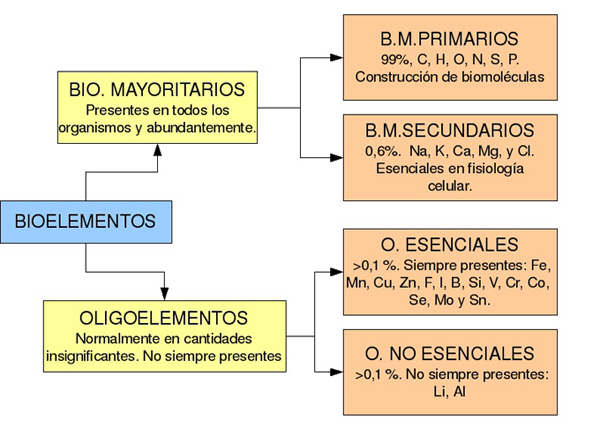
Son elementos químicos que forman parte de los seres vivos. Aproximadamente hay unos 70 bioelementos que se agrupan en tres categorías:
BIOMOLÉCULAS
La combinación de los átomos de un bioelemento entre si con otros átomos de otro bioelemento, mediante elaces químicos, da lugar a diferentes moléculas que reciben el nombre de biomoléculas o principios inmediatos.
Las biomoléculas pueden ser:
- Inorgánicas: puede tener carbono o hidrógeno, pero nunca al mismo tiempo. Por ejemplo el agua, las sales minerales.
- Orgánicas: tiene que tener carbono e hidrógeno al mismo tiempo.
Por ejemplo los glúcidos, los lípidos, las proteínas, los ácidos nucleicos.
BIOMOLÉCULAS INORGÁNICASNo son exclusivas de los seres vivos, ya que también aparecen en la materia inerte. Son el agua y las sales minerales.
EL AGUA
El agua es la molécula más abundante de los seres vivos.Abundancia: 50 – 95%
Especies: Acuáticos – Desiertos / .........................................................
Edad: Embriones – Adultos / ...............................................................
Tejidos: Nervioso – Óseo /...................................................................
En el hombre el agua constituye el 65% del peso.
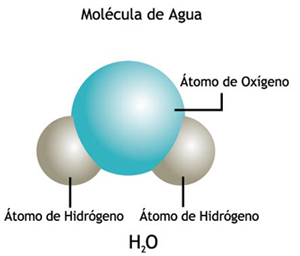
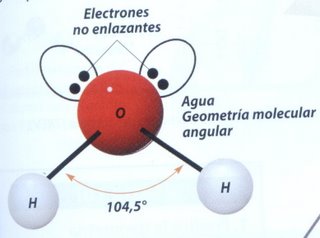
Estructura
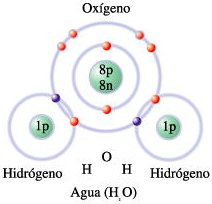
Una molécula de agua está formada por dos moléculas de hidrógeno y una molécula de oxígeno.
El oxígeno es un átomo muy electronegativo, por lo que atrae a los electrones hacia sí y se carga negativamente. Entonces el hidrógeno se carga positivamente. Por ello, la molécula de agua es dipolar, un polo es positivo (H) y un polo es negativo (O).
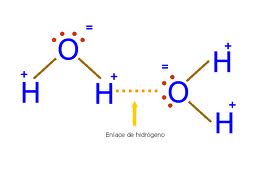
La consecuencia de que sea un dipolo, es que las moléculas de agua no están sueltas, sino que se unen entre ellas mediante los puentes o enlaces de hidrógeno que son enlaces débiles que seproducen entre un polo positivo y un polo negativo.
Enlaces de hidrógeno entre dos moléculas de agua
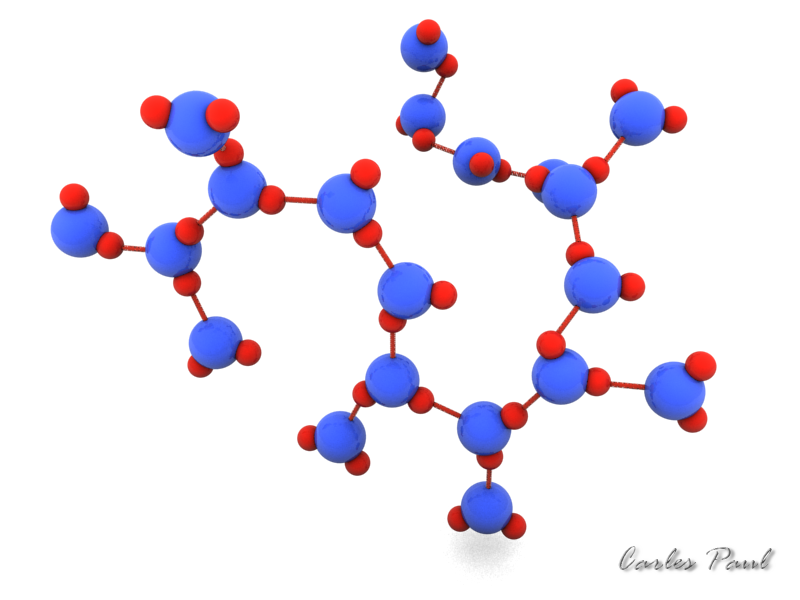
La masa molecular del agua es 18 por lo que a temperatura ambiente debería ser un gas, pero debido a los puentes de hidrógeno se unen muchas moléculas y hace que sea líquida a temperatura ambiente
Moléculas de agua enlazadas por enlaces de hidrógeno
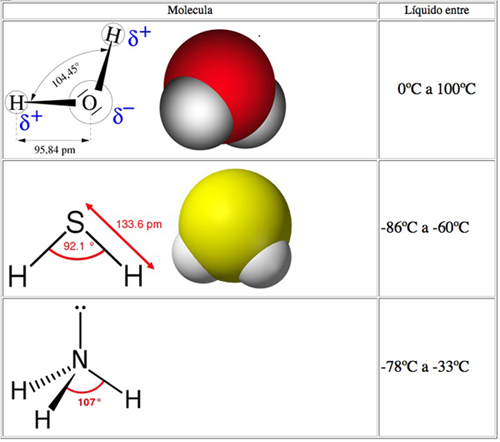
Comparación entre moléculas semejantes al agua y temperatura
a la que se encuentran en estado líquido
PropiedadesTodas las propiedades del agua son consecuencia de su estructura dipolar:
- Es el mejor disolvente de moléculas polares, porque debido a su carácter polar se forman enlaces de hidrógeno entre las moléculas de agua y las moléculas polares. Las moléculas que son solubles en agua se denominan hidrófilas. Y las moléculas que son insolubles en agua se llaman hidrófobas.
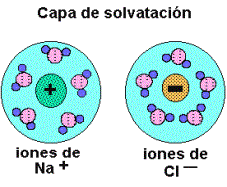
En el caso de las disoluciones iónicas los iones de las sales son atraídos por los dipolos del agua, quedando "atrapados" y recubiertos de moléculas de agua en forma de iones hidratados o solvatados.
- Este poder disolvente le convierte en un medio idóneo intracelular y extracelular para las reaccions químicas de los seres vivos.
- El agua tiene un elevado calor específico, es decir, las calorías que necesita un gramo de sustancia para aumentar su temperatura en 1ºC. Esta propiedad hace que el agua sea un buen agente termorregulador
- Elevada tensión superficial: permite deformaciones y movimientos citoplasmáticos. Desplazamiento en superficie

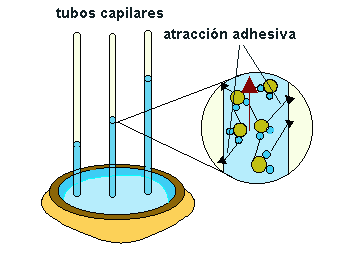
- Elevada fuerza de adhesión: Capilaridad. Importante en los vasos conductores de los vegetales
Funciones del agua en el organismo
Intimamente relacionadas con las propiedades anteriormente descritas, se podrían resumir en los siguientes puntos:
Reactivo químico y medio de reacción: En el agua de nuestro cuerpo tienen lugar las reacciones que nos permiten estar vivos. Forma el medio acuoso donde se desarrollan todos los procesos metabólicos que tienen lugar en nuestro organismo. Puede intervenir como reactivo en reacciones del metabolismo, aportando hidrogeniones (H3O+) o hidroxilos (OH -) al medio.
Función termorreguladora: Gracias a la elevada capacidad de evaporación del agua, podemos regular nuestra temperatura, sudando o perdiéndola por las mucosas, cuando la temperatura exterior es muy elevada es decir, contribuye a regular la temperatura corporal mediante la evaporación de agua a través de la piel.
Vehículo de transporte: Posibilita el transporte de nutrientes a las células y de las sustancias de desecho desde las células. El agua es el medio por el que se comunican las células de nuestros órganos y por el que se transporta el oxígeno y los nutrientes a nuestros tejidos. Y el agua es también la encargada de retirar de nuestro cuerpo los residuos y productos de desecho del metabolismo celular.
SALES MINERALES
Las sales minerales se encuentran en los organismos vivos de dos formas distintas:
- Disueltas (iónica): se encuentra disociada en aniones y cationes
Aniones: Cl- , PO43- , H PO42-, CO32- , NO3-
Cationes: Na+, K+, Ca2+, Mg2+, Fe2+, Fe3+
Funciones- Forman estructuras duras de los seres vivos.
- Regulan el equilibrio osmótico. Las membranas semipermeables son aquellas que dejan pasar el disolvente pero no el soluto. El equilibrio osmótico es el que hace que a ambos lados de una membrana semipermeable haya la misma concentración. Las membranas celulares de nuestras células son semipermeables.
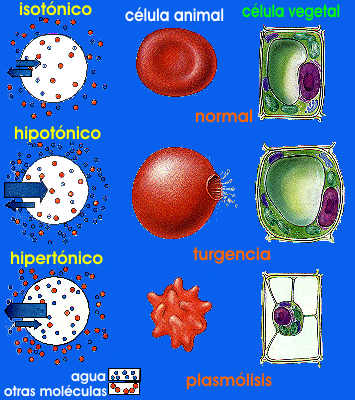
Cuando se ingiere mucha sal, el exterior de la célula se denomina extracelular hipertónico, que es donde se concentra toda la sal. Entonces, del interior de la célula, denominado intracelular hipotónico, sale el agua necesaria. Por ello, la célula se puede llegar a morir si no se ingiere agua rápidamente.
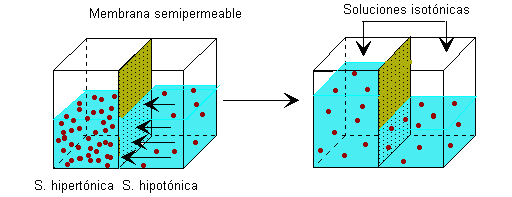
Cuando en el interior de la célula hay una mayor concentración de sal, se denomina intracelular hipertónica, entonces, del exterior, denominado extracelular hipotónico, entra agua para bajar la concentración. Pero si entra demasiada la célula se hincha y puede llegar a explotar y por lo tanto morir.
Lo normal es que la célula tenga la misma concentración dentro que fuera. El exterior de la célula se denomina extracelular isotónico.
- Regulan el equilibrio del pH. Para regular el pH existen los sistemas tampón, que consisten en aplicar un ácido débil o la sal correspondiente a ese ácido (todas las sales son neutras).
BIOMOLÉCULAS ORGÁNICAS
Son moléculas exclusivas (o casi) de los seres vivos. Están formadas por cadenas de carbono que forman estructuras lineales, ramificadas o cíclicas.
EL CARBONO gracias a sus cuatro electrones de valencia, es capaz de formar largas cadenas o esqueletos de muy diversas formas (lineales, ramificados o cíclicos)
También es capaz de formar más de dos enlaces covalentes estables con otros átomos (hasta cuatro)
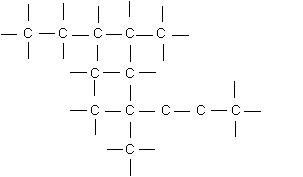
Ejercicio
Construir una molécula de 10 carbonos y completar con hidrógenos
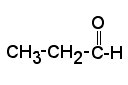
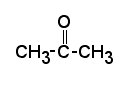
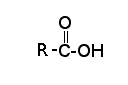
A estas cadenas se unen otros átomos como hidrógeno, oxígeno, azufre y fósforo dando lugar a diferentes grupos funcionales:
Ejercicio
Construir una molécula de 10 carbonos que incluya 5 grupos funcionales
con otros elementos químicos
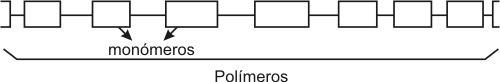
Monómeros y polímeros
Muchas moléculas orgánicas presentan una gran complejidad estructural y se denominan macromoléculas o polímeros. Estas macromoléculas se forman por la unión de moléculas menores, similares o idénticas, llamadas monómeros.
Según sus características, las biomoléculas se clasifican en glúcidos, lípidos, proteínas y ácidos nucleicos.