PROCESOS CATABÓLICOS IV
RESPIRACIÓN DE GLÚCIDOS (continuación)
El papel del NAD
En la glucolisis y en el ciclo de Krebs se han utilizado moléculas de NAD para "almacenar" los electrones que se han desprendido de las reacciones de oxidación correspondientes. Así que ahora tenemos los NAD en su forma reducida (NADH).
Pero la célula los necesita en su forma oxidada para que sigan funcionando como coenzimas en esas reacciones ¿Como resuelve la célula el problema de qué hacer con los electrones removidos por las reacciones de oxidación?
Si bien las células pueden transferir electrones directamente desde el NADH al oxígeno, esto produciría directamente la liberación de la energía como calor.
c) Cadena de transporte electrónico
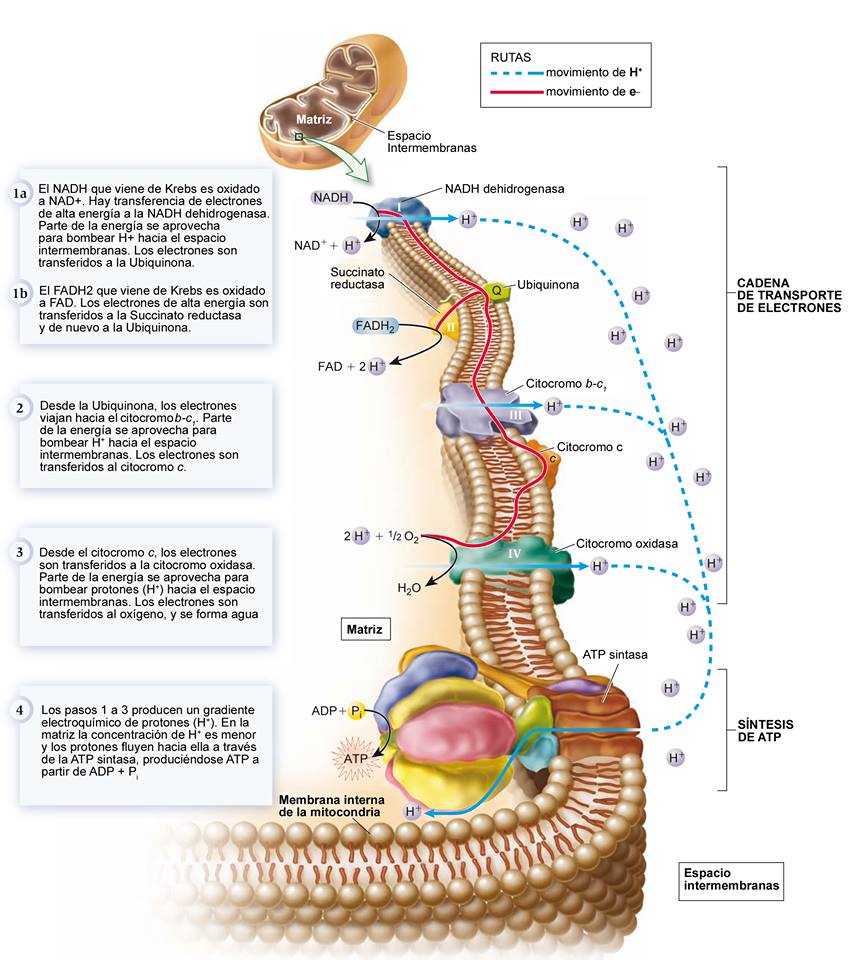
El transporte de electrones en la cadena respiratoria es la última etapa de la respiración.
En ella se van a oxidar las coenzimas reducidas (NADH y FADH2) producidas en las etapas anteriores y de esta forma van a ser utilizadas para sintetizar ATP a partir de la energía que contienen (síntesis de ATP por fosforilación oxidativa), a la vez que van a recuperar su forma oxidada.
Si bien, en las fases anteriores (glucolisis y ciclo de Krebs) el oxígeno no es necesario, en esta fase se requiere la presencia obligada de condiciones aerobias (presencia de oxígeno)
¿Por qué? Porque el oxígeno molecular, el que respiramos, va a ser la última molécula aceptora de la cadena de transporte de electrones para formar agua.
Se estima que la membrana interna de una mitocondria, en una célula hepática, tiene mas de 10.000 copias de cadenas transportadoras de electrones y complejos ATP sintetasas
La cadena de transporte electrónico la componen alrededor de 15 moléculas que se sitúan de forma ordenada en la membrana mitocondrial interna de las células eucariotas (también se encuentran en la membrana plasmática de las células procariotas). Cada una de estas moléculas acepta electrones de la molécula anterior, es decir, se reduce, y luego los transfiere a la molécula siguiente, por lo que se oxidará.
Esto es posible porque los electrones siempre pasan a ocupar en la siguiente molécula una posición más próxima al núcleo, es decir, de menor energía.
Los electrones que entran en la cadena respiratoria proceden de los NADH y FADH2 que, al cederlos junto con los protones (H+), pasan a ser las coenzimas oxidadas NAD+ y FAD, respectivamente.
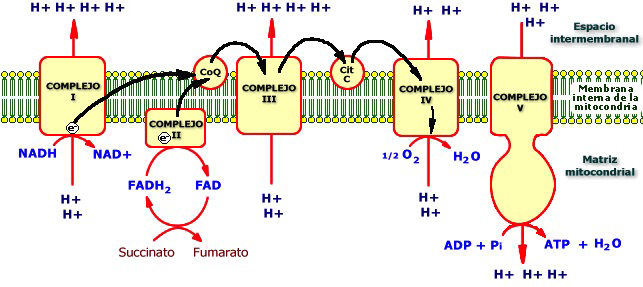
La cadena respiratoria está formada principalmente por cuatro complejos enzimáticos y varios transportadores:
Complejos enzimáticos implicados en la cadena transportadora de electrones: Los cuatro complejos están unidos a la membrana interna mitocondrial.
- Tres de ellos son complejos transmembrana (embebidos en ella): el I, el III y el IV y tienen la capacidad de actuar como bombas de protones. Cada uno de estos complejos posee un potencial redox cada vez más positivo que el anterior.
- El otro complejo, el Complejo II solo está asociado a ella y no bombea H+.
Transportadores implicados en la cadena transportadora de electrones
- Ubiquinona (UQ, Q o CoQ): molécula lipídica capaz de trasladarse por la doble capa lipidica de la membrana mitocondrial interna y que tiene la función de transportar electrones del complejo I y II al III
- Citocromo c: está en la cara interna de la membrana y que comunica el complejo III con el IV
Y a todo ello hay que añadir la ATP sintetasa que también está formada por un complejo multienzimático (a veces referida como el complejo V)
- El "complejo I" o NADH deshidrogenasa está formado por varias cadenas polipeptídicas que utilizan nucleótidos de flavina y adenina como coenzimas. Éste complejo enzimático capta dos electrones del NADH y los transfiere a un transportador liposoluble denominado ubiquinona (UQ)
- El "Complejo II" o Succinato deshidrogenasa, no es un bomba de protones. Es la única enzima del ciclo de Krebs asociado a membrana. Este complejo dona electrones a la ubiquinona desde el succinato (que se transforma en fumarato) y los transfiere a la ubiquinona mediante el FAD.
- El "complejo III" o Complejo Citocromo b-c1 o Citocromo reductasa obtiene 2 electrones desde UQH2 y se los transfiere a dos moléculas de citocromo c.
- El “complejo IV” o Citocromo c - oxidasa, capta los electrones de las cuatro moléculas de citocromo c y se transfieren al oxígeno (O2), para producir dos moléculas de agua (H2O). Al mismo tiempo se translocan cuatro protones al espacio intermembrana, por los cuatro electrones.
¿Como se realiza el transporte de electrones?
El transporte de electrones se va a realizar a través de una serie de reacciones de OXIDO-REDUCCION. En cada reacción intervienen dos componentes de la cadena respiratoria con potenciales redox diferentes.
Potencial redox (E): es una medida de la afinidad del transportador por los electrones y se mide en VOLTIOS. Cuanto más positivo sea, mayor afinidad tiene. Y cuanto mayor sea la diferencia de potencial redox entre dos transportadores, mayor va a ser la energía liberada en el transporte de electrones, energía que va ser utilizada por la ATP SINTETASA para la formación de ATPs
El transporte de electrones se inicia cuando una molécula de NADH o de FADH2 se oxida y cede electrones y H+ a uno de esos complejos multienzimáticos. A partir de ese momento, los electrones se van a transportar-desplazar desde el complejo con potencial redox más negativo a uno más positivo o menos negativo. De esta manera los electrones van a ir "descendiendo" en cascada hacia los complejos situados en niveles energéticos más bajos hasta llegar finalmente al oxigeno reduciéndolo y formando agua.
Cabe aclarar que los tres primeros aceptores reciben el H+ y el electrón conjuntamente. En cambio, a partir del cuarto aceptor, sólo se transportan electrones, y los H+ quedan en solución.
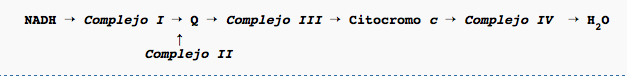
El flujo de electrones en el proceso sería del siguiente modo:
- Los e- captados por el NADH entran en la cadena cuando son transferidos al complejo I, que se reduce y los transfiere a la coenzima Q (Co Q). El complejo I vuelve a su forma oxidada, para recibir otro par de electrones, y la Co Q se reduce. A continuación, la Co Q cede los e- al siguiente aceptor, el Complejo III y vuelve a su forma oxidada
- A la cadena respiratoria también se puede acceder “lateralmente” mediante el complejo II, que utiliza el FADH2, cuyos electrones entran en la cadena, en un nivel energético ligeramente inferior a los del NADH.
- El proceso se repite en sentido descendente. Al pasar los e- por la cadena respiratoria, van saltando a niveles energéticos sucesivamente inferiores elect.
- Finalmente los e- llegan hasta el O2, que se combina con 2 protones, para formar agua que sale de la mitocondria y de la célula.
El oxígeno es fundamental en el proceso pues sin él, el último componente de la cadena no podría volver a oxidarse una vez reducido, ya que no tendría ningún par redox al cual entregar los e-. Gracias a que el O2 del ambiente acepta los electrones, el proceso puede continuar
Hipótesis quimiosmótica: fosforilación oxidativa
El flujo de electrones está íntimamente acoplado al proceso de fosforilación, y no ocurre a menos que también pueda verificarse este último. Esto, en un sentido, impide el desperdicio de energía, ya que los electrones no fluyen a menos que exista la posibilidad de formación de ATP.Si el flujo de electrones no estuviera acoplado a la fosforilación, no habría formación de ATP y la energía de los electrones se degradaría en forma de calor.
Puesto que la fosforilación del ADP para formar ATP se encuentra acoplada a la oxidación de los componentes de la cadena de transporte de electrones, este proceso recibe el nombre de fosforilación oxidativa.
Durante mucho tiempo se intentó explicar la naturaleza del enlace entre la cadena respiratoria y el sistema de fosforilación. En 1961, Mitchell propuso la hipótesis quimiosmótica, que es la que actualmente se acepta en general. Esta hipótesis ha sido apoyada por las evidencias experimentales encontradas en distintos laboratorios, lo que le valió a Mitchell el premio Nobel en 1978.
La misma propone que el transporte de electrones y la síntesis de ATP están acopladas por un gradiente protónico a través de la membrana mitocondrial (gradiente electroquímico). El proceso transcurre en dos etapas:
1.- Formación de un gradiente de protones a un lado y otro de la m. mitocondrial interna
En tres transiciones de la cadena de transporte de electrones (en los complejos I, III y IV) se producen caídas importantes en la cantidad de energía potencial que retienen los electrones, de modo que se libera una cantidad relativamente grande de energía libre en cada uno de estos tres pasos que se utiliza para bombear H+ al espacio intermembrana de la mitocondria (4, 4 y 2 H+ respectivamente).
Los electrones transportados por la NADH entran en la cadena cuando son transferidos a la FMN, que entonces se reduce.
Los electrones que son transportados por el FADH2 se encuentran en un nivel energético ligeramente inferior que los del NADH. En consecuencia, entran en la cadena de transporte más abajo, a la altura de la CoQ.
1 NADH = 3 ATP
1 FADH2 = 2 ATP
Según este modelo, el transporte de electrones paso a paso, desde el NADH o el FADH2 hasta el oxígeno a través de los transportadores de electrones, da por resultado el bombeo de protones a través de la membrana mitocondrial interna hacia el espacio entre las membranas mitocondriales interna y externa.
Este proceso genera un potencial electroquímico de membrana a través de la membrana mitocondrial interna, ya que el medio que ocupa el espacio intermembranoso se carga positivamente.
La diferencia en concentración de protones entre la matriz y el espacio intermembranoso representa energía potencial, resultado en parte de la diferencia de pH y en parte de la diferencia en la carga eléctrica de los lados de la membrana.
2.- Utilización del gradiente de protones para formar ATP (fosforilación oxidativa)
Cuando los protones pueden fluir de regreso a la matriz, descendiendo por el gradiente protónico, se libera energía utilizable en la síntesis de ATP a partir de ADP y Pi.
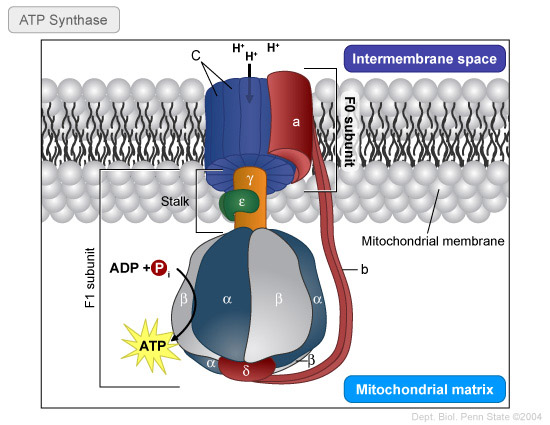
Los protones regresan a la matriz a través de conductos especiales situados en la membrana interna. Estos conductos están formados por un gran complejo enzimático, llamado ATP sintetasa (o sintasa).
Este complejo consta de dos partes: F0 y F1 (ver estructura mitondrias). Las partículas F0 están incluidas en la membrana mitocondrial interna y la atraviesan desde afuera hacia adentro.
Poseen un conducto o poro interior que permite el paso de los protones y que aprovecha el paso de protones para llevar a cabo la síntesis de ATP a partir de ADP y Pi. De esta manera, el gradiente protónico que existe a través de la membrana mitocondrial interna acopla la fosforilación con la oxidación.
Quimiósmosis (hipótesis quimiosmótica) en la mitocondria. Obsérvese el bombeo de protones desde la matriz mitocondrial al espacio intermembrana (sombreado).
El ATP se forma del lado de la membrana que mira a la matriz, por la difusión de los H+ a través del complejo ATPsintetasa.
El movimiento de protones a favor del gradiente electroquímico, a medida que pasan a través del complejo de la ATP sintetasa, suministra la energía por medio de la cual se regenera el ATP a partir del ADP y el fosfato inorgánico
ver otra animación de la cadena de transporte electrónico
La Hipótesis Quimiosmótica es la hipótesis que explica el acoplamiento de ambos procesos, uno químico, de oxidación-reducción en la cadena de transporte electrónico y otro osmótico, de la creación de un gradiente electroquímico entre el espacio intermembranal y la matriz mitocondrial.
El resultado es la formación de ATP a través de la fosforilación oxidativa
BALANCE ENERGETICO GLOBAL DEL CATABOLISMO AEROBIO
Una vez entendido y explicado el proceso completo de la respiración celular podemos hacer un balance total del rendimiento obtenido por cada molécula de glucosa.
Por cada NADH que llega a la cadena respiratoria, cede un par de electrones que en su transporte liberan energía suficiente para bombear 10 H+ (4, 4 y 2 H+) desde la matriz al espacio intermembrana (complejos I, III y IV).
Y por cada FADH2 que llega a la cadena de transporte electrónico, como cede los electrones a un componente de la cadena posterior (complejo II), solo se producen 6 H+ (4 y 2 H+).Por cada 3 H+ que vuelven a entrar a la matriz se obtiene energía suficiente como para que la ATP sintetasa sea capaz de fosforilar un ADP + P produciendo 1 ATP
Con fines prácticos, aunque no es del todo exacto, se considera que una molécula de NADH permite la formación de 3 moléculas de ATP (10 H+), mientras que una de FADH2 sólo aportará 2 ATP (6 H+)
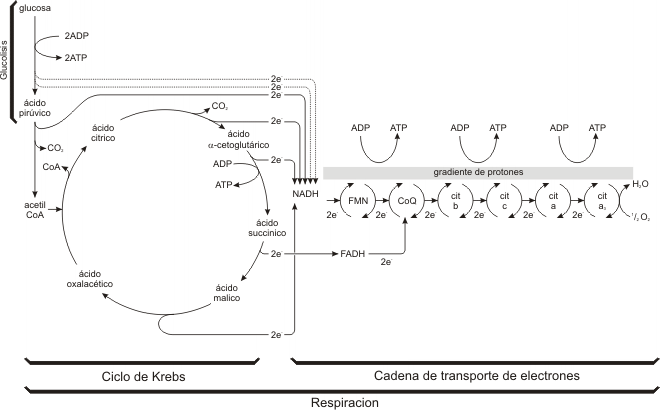
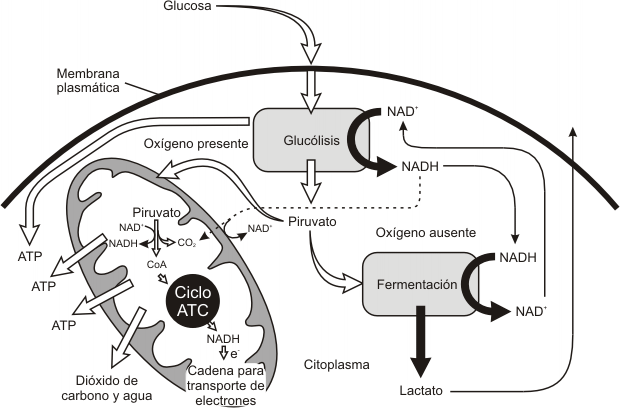
Relación entre la glucolisis-ciclo de Krebs y la cadena de transporte electrónico
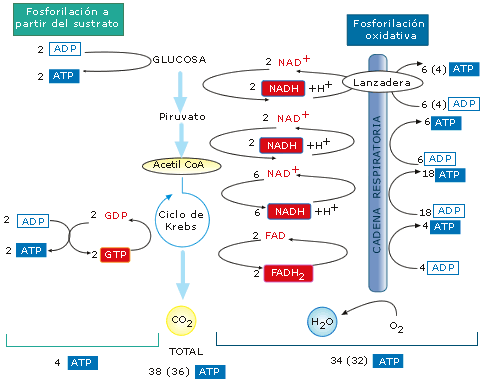
Balance de la respiración celular de una molécula de glucosa
Así, el balance para una molécula de glucosa que se convierte en 2 piruvatos, luego en 2 Acetil-CoA y luego a CO2 en la vía el ciclo de los ácidos tricarboxílicos, con todo el NADH y el FADH convertidos en ATP por la cadena de transporte electrónico:
1 glucosa + 38 ADP + 38 Pi6 CO2 + 38 ATP
Nota: los 2 NADH que se forman en el citoplasma durante la glucólisis, para ser transportados a la matriz mitocondrial y ser posteriormente oxidados por la cadena transportadora de electrones, tienen que pasar por medio de transporte activo a traves de la membrana mitocondrial interna al interior de la mitocondria.Esto "cuesta" 1 ATP por NADH que entra en la mitocondria
ver lanzaderas para la entrada en la mitocondria del NADH
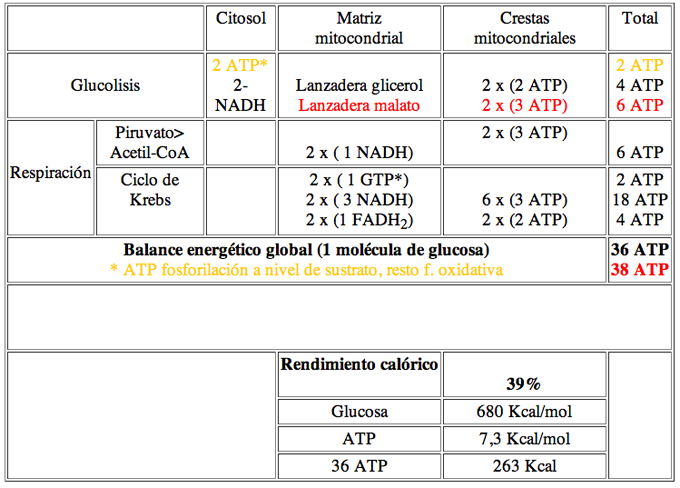
Por lo tanto el balance final resulta en 36 ATP por glucosa y no 38 ATP.
ver animación balance energético respiración glúcidos
Rendimiento energético de la respiración celular
Las células podrían transferir electrones directamente desde el NADH al oxígeno, pero esto produciría directamente la liberación de la energía como calor.
NADH + O2 -------> NAD + H2O
Go' = -52 kcal/mol
Si el NADH tiene ~52 kcal de energía, y solo son necesarias 7,3 kcal para hacer un ATP, se puede calcular en 52/7,3 = ~ 7 ATP por NADH si la conversión de energía fuese de un 100% de eficiencia.En la práctica las células han desarrollado sistemas que le permiten obtener hasta un 40% de eficiencia (~3 ATP/NADH) bajo condiciones óptimas.
Expresado de otro modo: la eficiencia de la respiración llega casi al 40% de la energía presente inicialmente en la molécula de glucosa, y es conservada en forma de ATP; el resto se libera como calor
CATABOLISMO AEROBIO DE OTROS AZÚCARES
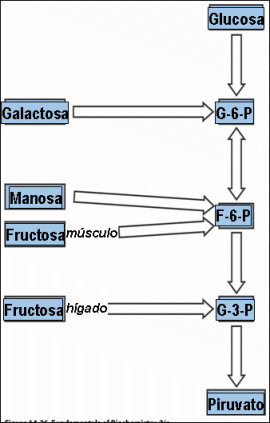
Otros azúcares como fructosa, galactosa... también pueden degradarse para obtener energía ya que tienen sus propias vías de entrada en la glucólisis.
Vías de entrada de diferentes monosacáridos al catabolismo de los azúcares
ESQUEMA GENERAL DE TODO EL CATABOLISMO DE GLÚCIDOS
ver vídeo respiración celular (2)
ver balance respiración celular
ver animación catabolismo glúcidos: respiración celular y fermentación